泌尿系统肿瘤是威胁中老年男性健康的常见“杀手”,其中,膀胱癌作为泌尿系统第一大恶性肿瘤,位列我国男性恶性肿瘤发病率第七[ 郑荣寿,孙可欣,张思维等。2015年中国恶性肿瘤流行情况分析[J]。中华肿瘤杂志,2019,41(1):19-28。],且呈逐年上升趋势,而膀胱癌中约90%以上为尿路上皮癌[ 中华人民共和国国家卫生健康委员会。 膀胱癌诊疗规范(2018年版)。]。
长期以来,尿路上皮癌面临确诊晚、易复发、治疗手段有限等困境,在泌尿系统肿瘤中,尿路上皮癌患者的预后生存率远低于前列腺癌和肾癌。随着肿瘤生物学机制研究的深入,以程序性细胞死亡-1(PD-1)及其配体(PD-L1)抑制剂为代表的免疫治疗在尿路上皮癌治疗中取得了突破性进展,极大地提升了临床疗效并改善患者生存质量。
近日,罗氏诊断PD-L1 (SP263)抗体检测(免疫组织化学法)作为国内首个尿路上皮癌免疫治疗伴随诊断在华获批上市,标志着我国正式开启尿路上皮癌免疫诊疗时代。罗氏诊断中国总经理姚国樑先生指出:“继去年亮相第二届中国国际进口博览会后,很高兴PD-L1 (SP263)伴随诊断正式落地中国,这是罗氏诊断在中国推行个体化医疗策略的又一重要里程碑,希望该检测能够为临床制定医疗决策提供可靠依据,帮助患者实现获益最大化。”
 PD-L1 (SP263)伴随诊断上市仪式
PD-L1 (SP263)伴随诊断上市仪式易转移、易复发、预后差 免疫疗法打破膀胱癌治疗困境
膀胱癌可见于各年龄段,发病率随着年龄的增长而增加,高发年龄为50~70岁,男性发病率约为女性的3.3倍2。由于膀胱癌患者早期往往没有明显的临床体征,约10%~15%的膀胱癌患者在初次确诊时已发生转移,且约50%经根治性膀胱切除术的患者在术后出现复发或转移;对于转移性膀胱尿路上皮癌患者,首选的治疗方法是含铂类药物的联合化疗方案,即一线治疗,其总体反应率为50%左右,由于化疗药物敏感性下降等原因,几乎所有患者都会发生疾病进展,中位生存时间约为14个月,五年生存率仅5%~20%2。
北京大学第一医院泌尿外科虞巍教授介绍道:“近年来,许多常见的恶性肿瘤在治疗方面都取得了长足的进步。而尿路上皮癌因具有易转移、易复发等特点,且对于经标准化疗方案失败的患者二线治疗方案选择有限,患者长期生存率多年来一直没有太大的改善。随着越来越多免疫治疗临床试验得出积极数据,尿路上皮癌的治疗迎来了新的突破口。相较于化疗,免疫治疗显著降低了晚期及转移性尿路上皮癌患者疾病进展或死亡的风险,总生存率得到明显提升[ Fradet Y,Bellmunt J,Vaughn D J et al。 Ann。 Oncol。 2019 May 03。]。”
不同于传统化疗手段,基于PD-1/PD-L1抑制剂的免疫治疗通过增强或正常化人体自身免疫系统抑制和杀伤肿瘤细胞,治疗相关不良事件发生率更低,安全性更高[ Bellmunt J, et al。 N Engl J Med。 2017;376:1015-1026。],是当前最具前景的肿瘤精准医疗发展方向之一。
“免疫疗法作为晚期及转移性尿路上皮癌二线治疗方案,能够为一线治疗失败的患者提供更好的生存获益。”虞巍教授指出,“除此之外,不同的免疫治疗联合方案和标志物筛选策略在一线和新辅助方面的研究仍在探索,未来也期待有充足证据能支持更前线的治疗获益。”
伴随诊断锁定PD-L1高表达患者 最大化免疫治疗效果
需要注意的是,并非所有的尿路上皮癌患者都能从免疫治疗中获益。研究显示,若对患者不加选择地使用PD-1/PD-L1抑制剂进行治疗,其整体有效率仍然偏低[ Rosenberg et al。 Lancet 2016],[ Apolo et al。 ASCO GU 2016]。因此,临床亟需通过合适的生物标志物检测预估患者的免疫治疗潜在获益情况,从而筛选出真正可能获益的患者给予治疗。
浙江大学医学院附属第一医院病理科滕晓东教授强调:“精准诊断是精准医学的先决条件。多项研究证实,PD-L1高表达患者的免疫治疗获益更明确,PD-L1表达水平的精准评估对于疗效评估、避免低效或无效的临床诊疗决策至关重要。作为肿瘤个体化医疗必不可少的组成部分,PD-L1伴随诊断在免疫治疗临床病理实践中扮演日益凸显的重要角色,相应的标准化要求也越来越高。”
目前,免疫组织化学法(IHC)是临床实践中唯一经试验验证、法规审批用于伴随诊断级别评估PD-L1表达水平的方法学[ Tsao, MING SOUND, et al。 IASLC atlas of PD-L1 immunohistochemistry testing in lung cancer。 Aurora, CO: International Association for the Study of Lung Cancer (2017)],[ 2018 ESMO handbook of immune-oncology。]。与此同时,作为病理实验室常规开展的成熟项目,IHC相较其它方法学具有较明显的经济、快速、易于开展的优势。
“作为国内首个尿路上皮癌免疫治疗伴随诊断,期待PD-L1 (SP263)的上市能推动尿路上皮癌免疫诊疗实践,积累更充分的实践证据。”滕晓东教授评价道,“免疫治疗的发展正迅速改变着多种肿瘤的诊疗模式,在为临床带来新的治疗选择的同时也对病理诊断提出了更多挑战。PD-L1的表达不同于传统靶向治疗相关标志物有或无的特征,往往具有连续性和不同部位可能存在异质性的特点。PD-L1检测标准的统一和结果的准确涉及检测体系的选择、实验室质控的评估以及判读共识等等[ Prince, Spasenija Savic, and Lukas Bubendorf。 Predictive potential and need for standardization of PD-L1 immunohistochemistry。 Virchows Archiv 474.4 (2019): 475-484。],[ Lantuejoul, Sylvie, et al。 PD-L1 Testing for Lung Cancer in 2019: Perspective From the IASLC Pathology Committee。 Journal of Thoracic Oncology (2019)。],相应规范化建设任重而道远。”
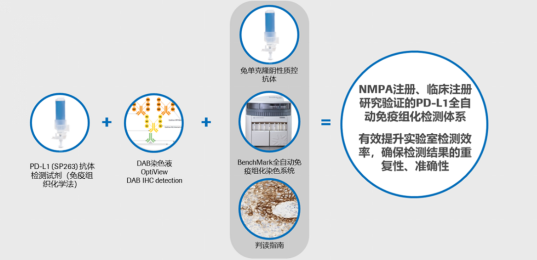 PD-L1 (SP263)获批伴随诊断涉及整个检测体系
PD-L1 (SP263)获批伴随诊断涉及整个检测体系据悉,PD-L1 (SP263)伴随诊断是当前国际上关联免疫治疗药物最多的伴随诊断,涵盖两款尿路上皮癌及三款非小细胞肺癌PD-1/PD-L1抑制剂8,10,[ VENTANA PD-L1 (SP263) Assay (CE IVD) Package Insert。],[ https://fda.report/PMA/P160046]。“尿路上皮癌是PD-L1 (SP263)伴随诊断在中国上市的首个适应症,适用于罗氏诊断BenchMark全自动IHC染色平台。相信随着今后该检测的更多适应症在中国获批,更广大患者有望从中获益。”姚国樑先生表示。
 罗氏诊断中国总经理姚国樑先生
罗氏诊断中国总经理姚国樑先生最新鲜的上海生活资讯!请扫描下方二维码关注官方微信















查看评论(0)网友评论
发 表 登录|注册